ایده دانشمند ایرانی که جایزه انجمن پژوهشهای علمی هلند به آن تعلق گرفت
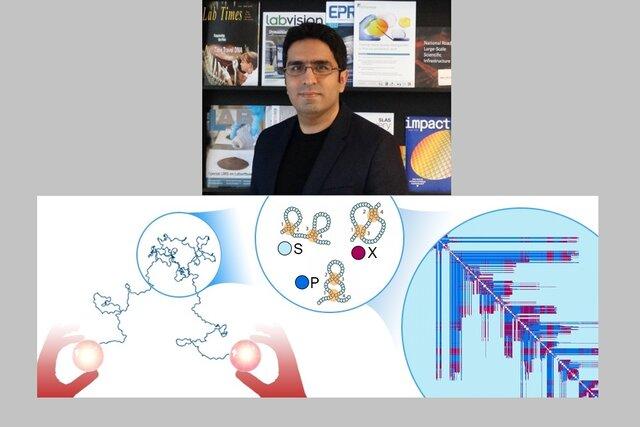
علیرضا مشاقی طبری، پزشک و دانشمند ایرانی و مؤسس مرکز پژوهشهای ژنومی دانشگاه لایدن هلند برنده جایزه پنجاه هزار یورویی انجمن پژوهشهای علمی هلند (NWO) شد. این جایزه به خاطر ایده ساخت دارو برای سرطان پروستات پیشرفته و مقاوم به درمان به وی تعلق گرفت.
پروفسور علیرضا مشاقی طبری، استاد دانشگاه لایدن هلند در گفتوگو با ایسنا، اظهار کرد: تولید دارو برای پروتئینهای نامنظم و عامل بیماریهای مقاوم به درمان، شاید یک ماموریت و مسئله غیرممکن به نظر برسد، اما تیم پژوهشی ما رهیافت نوینی را جهت حل این مسئله اتخاذ کرده است. پروژه ما توسط NWO در مسابقه ای که تحقیقات کنجکاوی محور و جسورانه (Open Competition ENW) را تشویق میکند، برنده شد.
وی توضیح داد: فرآیندهای بیولوژی در بدن انسان ازجمله رشد و متابولیسم، حرکت اندامها و پاسخ ایمنی در برابر عوامل بیماریزا عموما توسط پروتئینها انجام میشود. یک پروتئین برای انجام وظیفه، معمولا باید به شکل خاصی تا شود تا ساختار هندسی مشخصی داشته باشد.
"علیرضا مشاقی طبری، پزشک و دانشمند ایرانی و مؤسس مرکز پژوهشهای ژنومی دانشگاه لایدن هلند برنده جایزه پنجاه هزار یورویی انجمن پژوهشهای علمی هلند (NWO) شد"داروسازان از این اصل برای طراحی داروها استفاده میکنند. داروها طوری طراحی میشوند تا با شکل مشخصی از پروتئین مطابقت داشته باشند و به آن متصل شوند. تنها یک مشکل در این رویکرد وجود دارد؛ اگر پروتئین ساختاری نداشته باشد و نامنظم باشد، چه؟:
دکتر مشاقی تصریح کرد: نزدیک به یک سوم پروتئینهای ما نامنظم و یا دارای ناحیهای نامنظم هستند. آنها ظاهرا هیچ ساختاری ندارند و بسیار پویا هستند. برای این پروتئینها، ما به یک رویکرد اساسی جدید نیاز داریم.
بیشتر داروهای ما برای نواحی منظم طراحی شدهاند و برای آن دسته از داروهای کمیاب که ناحیه بی نظم را هدف قرار میدهند، ما هیچ ایدهای از نحوه عملکرد دارو نداریم.
مدیرگروه بیوفیزیک پزشکی و مهندسی زیستی در مرکز پژوهشهای دارویی لایدن، ادامه داد: هیچ دارویی برای سرکوب پروتئینهای نامنظم وجود ندارد. ناحیه بی نظم پروتئین اغلب برهمکنش پیچیدهای با سایر پروتئینهای سلولی ایجاد میکند که بسیار مهم است. به همین دلیل، آنها میتوانند در انواع مختلف بیماریها مانند دیستروفی عضلانی و انواع مختلف سرطان نقش داشته باشند. از جمله مهمترین این سرطانها میتوان به سرطان پروستات اشاره کرد که رشد آن وابسته به گیرنده هورمون آندروژن است.
دکتر مشاقی افزود: گیرنده هورمون آندروژن پروتئینی است که بیش از نیمی از این پروتئین نامنظم و بدون ساختار است. در مراحل اولیه سرطان پروستات، هورمون تستوسترون به قسمت منظم پروتئین متصل میشود و در آنجا رشد سرطان را تحریک میکند.
"این جایزه به خاطر ایده ساخت دارو برای سرطان پروستات پیشرفته و مقاوم به درمان به وی تعلق گرفت"بنابراین داروهای فعلی این قسمت منظم را هدف قرار میدهند و به آن متصل میشوند، جایی که رشد را مسدود میکنند. با این حال، در سرطان پیشرفته پروستات، سلولهای سرطانی پروتئینهای گیرندهای تولید میکنند که فاقد بخش منظم هستند. این به این معنی است که داروها دیگر نمیتوانند به پروتئین متصل شوند و گیرنده آندروژن رشد سرطان را بدون مزاحمت هدایت میکند؛ در حالی که داروها قادر به سرکوب آن نیستند.
این استاد و پژوهشگر وابسته به دانشگاه هاروارد آمریکا، خاطرنشان کرد: رویکردهای فعلی ناکافی است. رویکردهای تجربی و محاسباتی مورد استفاده در حال حاضر برای مطالعه پروتئینهای نامنظم مناسب نیستند. حتی پیشرفتهای اخیر در فناوریهای محاسباتی مانند رویکرد هوش مصنوعی گوگل (alpha-fold) نیز قادر به حل مساله ساختار پروتئینهای بینظم نیست.
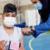
به همین دلیل، تیم تحقیقاتی ما با یک راه حل میان رشتهای برای این مساله، کار تحقیقاتی انجام داده است که ترکیبی از فناوریهای محاسباتی و آزمایشگاهی جدید است. با کمک این روشها میتوان ابتدا پویایی این زنجیرهها را درک کرد و سپس راهی پیدا کرد تا دینامیک نامطلوب را به پویایی مطلوب تبدیل کرد. به عبارت دیگر این رویکرد جدید به دنبال یافتن نظم در هرج و مرج است.
مؤسس مرکز پژوهشهای ژنومی دانشگاه لایدن هلند، خاطرنشان کرد: برای حل این مشکل از ماشینهای زیستی پیچیده به نام "چاپرون مولکولی" الهام گرفته شده است که این مولکولها در سلولهای ما با گرفتن یک زنجیره پروتئینی تاشو با زائدههایشان یا محصور کردن آن، دینامیک کل زنجیره را تنظیم میکنند. با الهام از طبیعت و تقلید آن ما میتوانیم پس از یافتن نظم در این پروتئینهای بینظم، "چاپرونهای مولکولی" مصنوعی بسازیم که بتوانند توپولوژی پروتئین را کنترل کنند. این چاپرونهای مصنوعی میتوانند بهعنوان نوع جدیدی از داروها عمل کنند که توپولوژی بد را سرکوب و یک نوع خوب را ترویج میکنند.
"یک پروتئین برای انجام وظیفه، معمولا باید به شکل خاصی تا شود تا ساختار هندسی مشخصی داشته باشد"در صورت موفقیت، میتوانیم رویکرد خود را در مورد بسیاری از پروتئینهای بینظم دیگر که در انواع بیماریها دخیل هستند، اعمال کنیم.
به گزارش ایسنا، پروفسور علیرضا مشاقی، استاد دانشگاه لایدن هلند و مدیر گروه مهندسی زیستی در موسسه پژوهشهای دارویی لایدن در زمینه بیماریهای ناشی از بدتاخوردگی پروتئینها از جمله سرطان و بیماریهای عصبی عضلانی و نیز ساخت اندام تراشه برای مطالعه بیماریهای ویروسی و ایمنی پژوهش میکند.
مشاقی پس از گذراندن دوره دبیرستان وارد دانشکده پزشکی دانشگاه تهران شد و به عنوان اولین دانشجوی تحصیلات همزمان کشور مدرک دکترای پزشکی و لیسانس و فوق لیسانس خود را در همین دانشگاه و در رشته شیمی و بیوفیزیک گرفت. سپس در دانشگاه صنعتی شریف در دوره کارشناسی ارشد فیزیک تحصیل کرد.
وی در سال ۲۰۰۸ میلادی دوره پست مستر را در دانشگاه فدرال زوریخ (ETH) در رشته مهندسی مواد به پایان رساند و موفق به اخذ مدرک دکتری با درجه ممتاز در رشته علوم نانو و فیزیک از دانشگاه صنعتی دلفت شد. وی همچنین در دانشکده پزشکی هاروارد دوره فلوشیپ چشم پزشکی را به پایان برد.
مشاقی در دانشگاههای مختلفی از جمله دانشگاه هاروارد، دانشگاه ام ای تی، دانشگاه استنفورد و دانشگاه تهران تدریس و پژوهش کرده است. وی بهویژه در جهت رشد پژوهش و آموزش میان رشتهای در ایران بسیار فعال بوده و قانون تحصیلات همزمان آموزش عالی ایران به همت وی تدوین و تصویب شده است.
پروفسور مشاقی به عنوان محقق و دانشمندی برجسته برنده جایزه یک میلیون و ۲۰۰ هزار دلاری سازمان پژوهشهای ملی هلند برای پژوهشهای تکسلولی بر روی سرطان و نیز جایزه ۳۰۰ هزار دلاری مرکز دیستروفی عضلانی آمریکا شده است. وی در سال ۲۰۱۸، به خاطر پژوهشهای بینرشتهای و تکمولکولی به عنوان کاشف سال انتخاب شد.
یک تیم پژوهشی بینالمللی به سرپرستی این دانشمند ایرانی موفق به حل مساله توپولوژی پروتئینها پس از حدود نیم قرن شد.
انتهای پیام
اخبار مرتبط
دیگر اخبار این روز
حق کپی © ۲۰۰۱-۲۰۲۴ - Sarkhat.com - درباره سرخط - آرشیو اخبار - جدول لیگ برتر ایران